| Titel: | Beschreibung des neuen Kupferhüttenprocesses der Bergwerks-Ingenieure Rivot und Phillips. |
| Fundstelle: | Band 118, Jahrgang 1850, Nr. XXIV., S. 106 |
| Download: | XML |
XXIV.
Beschreibung des neuen Kupferhüttenprocesses der
Bergwerks-Ingenieure Rivot und Phillips.
Mit Abbildungen auf Tab.
II.
Beschreibung des Kupferhüttenprocesses von Rivot und
Phillips.
Wir haben über dieses neue Verfahren zur metallurgischen Behandlung der Kupfererze
zuerst eine Notiz im polytechn. Journal Bd. CV S.
187 und hierauf einen Bericht darüber von Pelouze in Bd. CVII S. 121 mitgetheilt, welchem wir nun aus den Annales des
Mines t. XIII mit Hülfe der Figuren 35, 36 und 37 eine
vollständigere Beschreibung nachfolgen lassen.
„Das neue Verfahren wurde zuerst in dem Laboratorium der Pariser
Bergwerksschule und dann in einem Flammofen zu Grenelle bei Paris angewendet.
Die HHrn. Rivot und Phillips lernten auf einer Reise durch England die Versuche kennen,
welche man in einer Kupferhütte angestellt hatte, um aus vorher gerösteten,
geschwefelten Erzen, durch galvanische Wirkung metallisches Kupfer zu gewinnen.
Die Beobachtungen, welche die Verfasser darüber machten, stimmten im Allgemeinen
mit den Bemerkungen überein, die Napier (polytechn.
Journal Bd. CIV S. 131) darüber
mitgetheilt hat. Man röstete die geschwefelten Erze vollkommen ab, brachte sie
alsdann in einen Ofen mit Graphitsohle in Fluß, und reducirte das Kupfer, indem
man durch das flüssige Metallsilicat einen starken galvanischen Strom gehen
ließ, den eines theils die Graphitsohle leitete und anderntheils eine gußeiserne
Platte, die über die Oberfläche der flüssigen Masse gehalten wurde.
Zuvörderst machten wir den Versuch, mittelst eines galvanischen Stromes nicht das
Kupfersilicat, sondern das reine Halbschwefelkupfer
zu reduciren. Es gelang uns über zwei Stunden einen constanten Strom durch das
geschmolzene und rothglühende Kupfersulfurid zu leiten. In einem gewöhnlichen
hessischen Tiegel brachten wir zwei kleine Stückchen von dichten Kohks an,
welche mittelst Kitt an den Wänden des Tiegels befestigt wurden. In diese
Kohksstückchen liefen zwei Platindrähte aus, welche wir mit den beiden Polen der
galvanischen Säule in Verbindung setzten. Die Platindrähte wurden gegen die
Einwirkung des Schwefels mittelst der Kohksstücke und des Kittes geschützt; denn
wir haben uns durch unmittelbare Versuche überzeugt, daß in der Rothglühhitze
die Kohks einen guten Leiter bilden, während es der Kitt in dieser Temperatur
fast gar nicht ist.
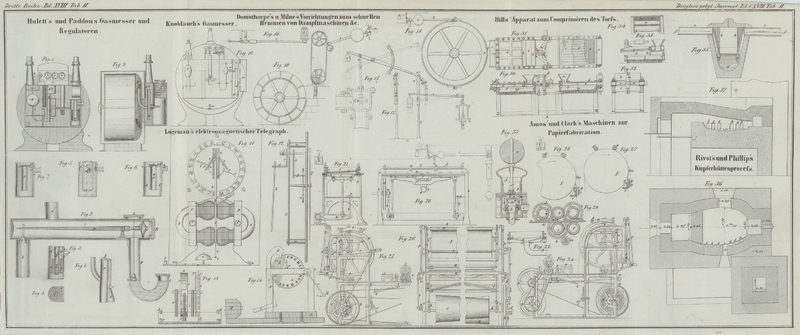
Die Einrichtung unsers Tiegels ist aus dem senkrechten Durchschnitte Fig. 35
ersichtlich. a, a sind die mit einer Säge
zugeschnittenen Kohksstücke; b, b ist der Kitt,
welcher dazu dient sie festzuhalten; d ist das
flüssige Halbschwefelkupfer, welches an die beiden Kohksstücke herantritt. f, f sind die beiden Platindrähte, welche in
Vertiefungen in den Kohksstücken auslaufen, und mittelst zweier Porzellanröhren
e, e durch den Ofen gehen.
Diese Röhren waren in zwei Ausschnitten im Tiegel angebracht, und ihr Zweck
bestand darin, die Berührung zwischen den Platindrähten und Kohlen zu
verhindern, welches aus zwei Gründen wesentlich war: 1) die glühenden Kohlen
würden eine Verbindung zwischen beiden Polen der außerhalb des Tiegels
angebrachten Säule herstellen, und es würde folglich ein bedeutender Theil der
Elektricität, wo nicht der ganze Strom, abgeleitet werden; 2) dann würde auch
die alkalische Asche der Holzkohle sehr schnell den Platindraht angegriffen
haben, und es würde dadurch der Strom unterbrochen worden seyn.
Wir haben Säulen mit constantem Strom und mit Kupfer- und Zinkelementen
von 6 bis 24 Paaren, mit Lösungen von Kupfervitriol und Kochsalz, zuweilen aber
auch nur eine Bunsen'sche Säule mit 30 Paaren
angewendet. Es wurden immer zwei Versuche gleichzeitig gemacht, indem wir in dem
Ofen stets zweiganzgleiche Tiegel anbrachten, von denen durch den einen
ein Strom ging und durch den andern nicht.
Mehrere Versuche ergaben, daß das Halbschwefelkupfer, welches durch Kohks nicht
zersetzt wird, mittelst einer Säule mit constantem Strom, die aus 24 Paaren
besteht und die Nadel des Galvanometers um 35 bis 40° ablenkt, eine nur
geringe Zersetzung erleidet. Wendet man eine Bunsen'sche Säule von 30 Paaren an, die am Galvanometer eine Abweichung
der Nadel von 45 bis 50° hervorbringt, so ist man im Stande einen
bedeutenden Theil Kupfer zu reduciren, wenn man den Strom länger als zwei
Stunden durch das geschmolzene Halbschwefelkupfer gehen läßt; der größte Theil
des Schwefelkupfers blieb aber unzersetzt.
Diese Versuche haben uns die Ueberzeugung geliefert, daß die Einwirkung der Säule
auf das Halbschwefelkupfer gering ist, und daß die zur Zersetzung desselben
erforderliche Intensität des galvanischen Stroms, sowie die Schwierigkeit, die
Apparate zweckmäßig einzurichten, eine Anwendung dieses Verfahrens beim
Kupferhüttenwesen verhindern müssen was hauptsächlich für den Kupferkies gilt,
der das gewöhnliche Kupfererz bildet.
Aehnliche Versuche, wobei wir die beiden Kohkspole durch Eisenstangen ersetzten,
haben uns die Ueberzeugung geliefert, daß zwar die Wirkung der Säule rascher
ist, jedoch nicht vollständig, und demnach die Reduction des Schwefelkupfers
durch Eisen ebensowenig im Großen angewendet werden kann, weil stets ein sehr
kupferreicher Stein zurückbleibt. Vom Kupferkiese trennen die eisernen Pole
verhältnißmäßig nur sehr wenig Kupfer.
Bei solchen Versuchen mit dem Bleiglanz zeigte derselbe ein ähnliches Verhalten
wie das Schwefelkupfer.
Später haben wir die Versuche von Napier wiederholt
und das flüssige Kupfer- und Eisensilicat durch einen Strom zu reduciren
gesucht, dessen einer Pol aus Eisen, der andere aus Graphit bestand, die in
unmittelbarer Berührung mit den geschmolzenen Substanzen standen. Wir
überzeugten uns aber, daß von den drei Agentien, welche in dem Tiegel zur
Reduction des Kupferoxyds angewendet werden, nämlich Graphit, Eisen und der
elektrische Strom, die beiden ersten, besonders aber das Eisen, schon
hinreichend waren.
Zahlreiche Versuche haben uns die Ueberzeugung gewährt, daß durch die Wirkung des
Eisens allein ein Kupfersilicat, welches außer dem Kupferoxyde auch noch andere
Basen, z.B. Natron und Kalk enthält, in sehr kurzer Zeit seinen ganzen Kupfergehalt abgibt,
der sich im Zustande völliger Reinheit als König sammelt.
Später haben wir den Versuch gemacht, das in einem geschmolzenen mehrfachen
Silicat enthaltene Kupferoxyd mittelst eines sehr kräftigen galvanischen Stroms
zu reduciren, der durch die flüssigen Substanzen mittelst zweier Platindrähte
geleitet wurde, die wenigstens einen Centimeter von einander entfernt waren. Wir
haben niemals die geringste Andeutung einer Reduction erlangt, nachdem wir
länger als zwei Stunden den constanten Strom einer Säule von 24 Paaren hindurch
gehen ließen.
Wir müssen demnach die Wirkung des Eisens als das Reductionsmittel des
Kupferoxyds betrachten.
Hierauf haben wir mehrere Versuche mit Tiegelschmelzen angestellt, um die
günstigsten Umstände für die Einwirkungen des Eisens zu erlangen, und sind
dadurch zu folgenden Hauptresultaten gelangt:
In unserm Tiegel waren zwei oder mehrere Eisenstäbe angebracht, die fast bis zum
Boden niedergingen, und oben durch eine Kittschicht festgehalten wurden.
Das Schmelzgut bestand entweder aus geröstetem Kupferkies oder aus einem Gemenge
von Eisenoxyd, Kupferoxyd und Sand. Als Zuschlag wendeten wir Soda oder ein
erdiges Glas, oder auch nur Kalkstein an. Wendet man Soda als Zuschlag an, so
erfolgt die Reduction des Kupferkieses in kurzer Zeit sehr vollständig und zur
Zerschmelzung ist nur 1/4 Stunde erforderlich; das gewonnene Kupfer ist chemisch
rein. – Mit Kalkstein oder erdigem Glase erforderte die vollständige
Reduction eine Schmelzdauer von einer Stunde; das gewonnene Kupfer war sehr
eisenhaltig (es enthielt bis 15 Proc. Eisen), wenn die Eisenstäbe bis zu dem
Kupferkönig reichten, und dagegen immer sehr rein, wenn diese Stäbe in einer
geringen Entfernung über dem König blieben. – Die zur vollständigen
Reduction des Kupferoxyds erforderliche Zeit war um so kürzer, je größer die
Anzahl der Eisenstäbe war.
In Folge dieser günstigen Resultate construirten wir einen Flammofen, der
ungefähr 250 Kilogr. oder 5 Centner geschmolzene metallische Silicate faßte und
weiter keine Eigenthümlichkeit hatte, als sechs senkrechte Vertiefungen in der
der Arbeitsthür gegenüberliegenden Wand, zu beiden Seiten der Abstichöffnung.
Diese Vertiefungen sind fünf Centimeter oder 2 Zoll tief und breit; sie fangen
etwa sechs Centim. über dem niedrigsten Punkte der Herdsohle an und reichen bis
auf einige Centimeter über den Spiegel des Metallbades, wie man aus den Figuren 36 und 37
ersieht. Der Zweck dieser Vertiefungen besteht darin, dicht über dem flüssigen
Metall sechs Eisenstäbe von 6 bis 8 Centimeter Höhe, 2 Centim. Dicke und 70
Centim. Länge zu erhalten. Diese Stäbe wirkten daher auf einer bedeutenden Höhe
des Metallbades, standen mit dem Kupfer nicht in Berührung und ließen sich
mittelst großer Zangen sehr leicht hinlegen und wieder wegnehmen. Auch gestatten
sie das Schmelzgut zwischen den Stäben umzurühren, um die mit dem Eisen in
Berührung stehenden Theile zu erneuern, so daß das Eisen mit der ganzen Masse in
Berührung kommen muß.
Wir haben in diesem Ofen mehr als 3800 Kilogr. Kupferkies aus Cornwallis,
Deutschland und Spanien, der vorher sehr sorgfältig geröstet worden war, zu Gute
gemacht.
Anfänglich wurden, nachdem das geröstete Erz mit Kalkstein und armen Schlacken
geschmolzen worden war, die sechs Stäbe alsdann in den Ofen gebracht und mußten
etwa vier Stunden lang wirken. Darauf wurden sie weggenommen und es wurde zum
Abstich geschritten. Dabei war aber der Eisenverbrauch weit größer als er nach
der Theorie zur Reduction des Kupferoxyds erforderlich wäre. Die Schlacken
hielten 2 bis 3 Procent Kupfer zurück.
Wir versuchten die Schlacken für sich allein zu verschmelzen und neue Eisenstäbe
darauf einwirken zu lassen, ebenfalls mit einer Dauer von vier Stunden. Dabei
fielen Schlacken, die ebenso reich an Kupfer waren wie bei dem ersten Schmelzen,
und dennoch hatten die Stäbe mehrere Kilogr. an Gewicht verloren.
Diese Oxydation der Eisenstäbe kann der directen Einwirkung der unverbrannten
Luft im Ofen auf das Eisen nicht zugeschrieben werden, weil dieselben
fortwährend und gänzlich von den geschmolzenen Materien umgeben waren; offenbar
aber dem Eisenoxyd, welches in dem Metallsilicat enthalten, und während der
Operation selbst durch die oxydirende Einwirkung der Flamme auf das mit der
Kieselerde verbundene Eisenoxydul gebildet worden ist, indem es durch das
metallische Eisen in den Zustand des Oxyduls zurückgeführt werden mußte, ehe
noch das Kupferoxyd vollständig durch das Eisen reducirt werden konnte.
Wir müssen hier einige Bemerkungen über die Bildung des Eisenoxyds in einer
flüssigen Schlacke mit Oxydulgehalt anreihen.
Bei den zahlreichen in unserm Flammofen angestellten Versuchen, wobei die
Brennmaterialschicht auf dem Rost sehr dünn und die Flamme daher sehr oxydirend
war, haben wir folgende Beobachtungen gemacht.
Da die Oberfläche der flüssigen Schlacke nicht mit Kohle bedeckt und folglich der
oxydirenden Einwirkung der Flamme überlassen war, so wurde die Schlacke sehr
bald dick und zähe, sobald die Temperatur des Ofens zunahm. Steckte man nun die
Eisenstäbe in diese zähe Schlacke, so wurde sie sehr bald wieder flüssig und es
verloren die Stäbe an ihrem Gewicht, ohne daß eine Reduction des Kupferoxyds
stattfand. Nahm man die Stäbe wieder weg, so wurde die Schlacke von Neuem
zähe.
Die Erklärung dieser Erscheinung ist unseres Erachtens einfach. Das mit der
Kieselerde in der flüssigen Schlacke verbundene Eisenoxydul oxydirt sich durch
die Flamme, wie man dieß bei der Auflösung eines Eisenoxydulsalzes, welches der
Luft ausgesetzt ist, sieht. Das gebildete Eisenoxyd gibt mit der Kieselerde eine
weniger flüssige Verbindung als das Oxydul, und die Schlacke muß daher steif
werden. Steckt man nun metallisches Eisen in eine solche Schlacke mit
Oxydgehalt, so wird das Oxyd auf Oxydul zurückgeführt, ehe das Eisen auf das
Küpferoxyd einwirken kann, und die Schlacke welche ungefähr 50 Procent
Kieselerde enthält, muß schnell viel flüssiger werden. Diese Einwirkung des
Eisens in hoher Temperatur auf die flüssigen Silicate, ist dem Verhalten dieses
Metalles zu den Metalllösungen analog; das Eisen fällt das Kupfer aus einer
Auflösung welche kein Eisenoxyd enthält, führt aber letzteres auf Oxydul zurück,
ehe eine Einwirkung auf das Kupfer stattfinden kann.
Die oxydirende Einwirkung der Flamme der Flammöfen auf die Schlacken mit
Eisenoxydul-Gehalt, welche bis jetzt nur wenig bekannt war, kann bei
verschiedenen Hüttenprocessen eine gewisse Wichtigkeit haben.
Wir versuchten daher den Eisenverbrauch zu vermindern und aus den Schlacken den
Metallgehalt noch mehr herauszuziehen, indem wir zu der Wirkung des Eisens noch
diejenige der Kohle fügten. Die Kohle konnte auf zweierlei Art angewendet
werden: 1) ein Gemenge mit dem gerösteten Erz; 2) oder als Zusatz zu den
vollständig geschmolzenen Silicaten. – Indem wir letzteres Verfahren
anwandten, konnten wir uns leicht überzeugen, daß die Kohle nur langsam und
schwach auf die flüssigen Silicate einwirke, da sie auf der Oberfläche der
flüssigen Masse schwimmt und nicht in ihr erhalten werden kann. Ihre Wirkung ist
aber durchaus nicht ganz Null, denn wenn wir auf die flüssige Masse eine gewisse
Quantität mageres Kohlenklein warfen, so bemerkten wir stets daß die Masse
schnell dünnflüssiger wurde, was sich nur dadurch erklären ließ, daß ein bedeutender
Theil des Eisenoxyds sich in Oxydul verwandelte. Da aber der Verbrauch an Eisen
hiebei noch bedeutend war, so vermengten wir die Kohle mit dem gerösteten Erz,
ehe es auf den Herd des Ofens gebracht wurde.
Nach einigen Versuchen gelangten wir zu folgendem zweckmäßigen Verhältniß von
Holzkohlenpulver oder von magern Staubkohlen. Es bestand nämlich in so viel
Kohle als durch Vereinigung mit dem Sauerstoff des Kupferoxyds und des
Eisenoxyds im gerösteten Erz zur Hälfte Kohlenoxyd und zur Hälfte Kohlensäure
liefern kann. Ein solches Verhältniß an zugeschlagener Kohle gab uns ohne
Benutzung von Eisen, Schlacken welche durchschnittlich 2 1/2 Procent Kupfer
enthielten. Durch mehrere Versuche sind wir noch zu folgenden Erfahrungssätzen
gelangt: 1) daß dieses Verhältniß der Kohle nicht genau genommen zu werden
braucht, sondern nicht unbedeutend vergrößert oder vermindert werden kann, ohne
daß die entstehende Schlacke ihren Kupfergehalt wesentlich verändert, oder die
Reinheit des gewonnenen Kupfers leidet;
2) daß bei einer bedeutenden Erhöhung des Verhältnisses der eingemengten Kohle
und bei einer Temperatur des Ofens bis zu einer lebhaften Weißglühhitze, wir die
letzte Schlacke immer noch ohne Einwirkung von Eisen bis auf 0,007 Kupfer
bringen konnten, wobei aber das Kupfer 8 bis 10 Proc. Eisen enthielt. Bei einer
geringern Temperatur erhielten wir aber eine sehr kupferreiche Schlacke, und
Kupfer mit einem Gehalt von 5 bis 6 Proc. Eisen.
3) Daß die Eisenstäbe auf ein flüssiges Metallsilicat von 2 bis 3 Procent
Kupfergehalt sehr stark und rasch wirken, und daß drei Stunden hinreichen, um
die Schlacken auf 0,004 bis 0,006 zu entkupfern und ein eisenfreies Kupfer zu
erzielen.
Nach allen diesen Versuchen blieben wir bei folgendem Verfahren stehen:
In den gehörig heißen Ofen wurde die Beschickung von 150 bis 170 Kilogr.
gerösteten Erzes mit Kalkstein (oder Schlacken von dem vorhergehenden Proceß)
eingetragen, und zwar mußten die Zuschläge von der Art seyn, daß die Beschickung
sehr bald in Fluß gerieth. Ein fernerer Zuschlag zu der Beschickung war
Holzkohlenstaub oder magere Staubkohlen, in dem oben angegebenen Verhältniß.
Sieht man in der ganzen Beschickung nur das Eisenoxyd und den Kalk als Vasen an,
so mußten wir ein Doppelsilicat mit einem Kalkgehalt von 12 bis 15 Proc.
hervorbringen. (Die Erfahrung hat uns gezeigt, daß ein Silicat, in welchem
Eisenoxydul die einzige Basis ist, sehr schnell schmilzt und sehr flüssig wird, aber auch
sehr leicht ein eisenhaltiges Kupfer liefert.) Nach dem Eintragen der
Beschickung warfen wir 1 oder 2 Schaufeln Kohlenklein auf die Oberfläche
derselben, um sie gegen die oxydirende Einwirkung der Ofenflamme zu schützen.
Von Zeit zu Zeit wurde das Schmelzgut umgerührt, wodurch eine gleichförmigere
Erhitzung und eine raschere Schmelzung veranlaßt wurde. Wir haben stets nach
vier Stunden eine vollständige Schmelzung erlangt.
Sobald das Schmelzgut zusammenzubacken anfängt, enthalten die Theilchen, welche
sich an die Brechstange anhängen, eine gewisse Menge von Kupferkörnern. Nach
erfolgter vollständiger Schmelzung zeigen die in das Schmelzgut eingeführten
Gezähe eine Vereinigung des Kupfers am tiefsten Punkte der Herdsohle in der Nähe
des Abstiches. Wir haben immer eine Probe von den Schlacken genommen, die auf
dem Kupfer in diesem Zeitpunkte des Processes schwammen, nachdem sie vorher
sorgfältig umgerührt worden waren, um eine recht gleichförmige Schlacke zu
erlangen. Diese Proben geben 2 bis 3 Procent Kupfer.
Nachdem alles gehörig geschmolzen war, führten wir sechs Eisenstäbe, welche
zusammen 36 bis 45 Kilogr. wogen, in den Ofen und legten ihre Enden in die oben
erwähnten Vertiefungen in der hintern Wand, so daß sie ganz von der flüssigen
Materie umgeben wurden. Darauf wurde von Neuem etwas Steinkohlenklein auf die
Schlacke geworfen, um die weitere Oxydation des in der Schlacke enthaltenen
Eisenoxyduls mittelst der Flamme zu bewirken. Dann wurde das ganze Schmelzgut
mit einem zweizinkigen Rechen eine halbe Stunde lang umgerührt, und mit diesem
Gezähe auch die in der Schlacke steckenden Eisenstäbe gereinigt. Als ein sehr
wirksames Mittel zum Umrühren wendeten wir auch eine hölzerne Stange an, welche
in die Schlacken gesteckt, Veranlassung zu einer bedeutenden Gasentwickelung und
zu einem starken Aufkochen gibt. Sobald die an Eisenoxydul sehr reiche Schlacke
nur noch 1 bis 2 Procent Kupfer gibt, kann ihr Ansehen nicht mehr dazu dienen,
den vorgerückten Stand der Reduction zu erkennen. Eine gute Probe ist jedoch
die, daß man eine kalte Brechstange einen Augenblick in die Schmelzmasse führt,
die sogleich einen röthlichen, metallischen Ueberzug bekommt, wenn die Schlacke
noch viel Kupfer enthält. Betrug aber der Kupfergehalt der Schlacken nur vier
bis fünf Tausendtheile, so zeigte die Brechstange diesen Ueberzug nicht.
Durch wiederholte Versuche haben wir gefunden, daß nach drei- bis
vierstündiger Einwirkung der Stäbe den Schlacken das Kupfer auf 0,0004 bis 0,006
entzogen war. Nach diesem Zeitraume nahmen wir die Stäbe heraus und schritten
zum Abstich. Die Dauer des Schmelzens beträgt demnach acht Stunden, so daß man
täglich drei Schmelzen vornehmen kann.
Der Gewichtsverlust des Eisens zeigte sich bei unsern Versuchen sehr verschieden,
indem er bei Kupfermengen von 12 bis 42 Kilogr., die aus Erzen von sehr
verschiedenartigem Metallgehalte dargestellt worden waren, bis 6 Kilogr. betrug.
Dieser Verlust ist übrigens von dem Gehalt des Erzes fast unabhängig und der
Eisenabgang ist verhältnißmäßig bei den reichen Erzen geringer als bei den
armen; bei den Kiesen aus Spanien mit 21 Procent Kupfergehalt betrug der Abgang
auf 100 Kilogr. gewonnenen Kupfers, 11 Kilogr. Eisen.
Die englischen Erze, welche wir verschmolzen, enthielten 7 Proc. Kupfer, 4 bis 6
Proc. Arsenik, etwas Antimon und einige Tausendtheile Zinn. Wir haben daraus ein
unreines Schwarzkupfer gewonnen, welches 3 bis 5 Proc. Arsenik, 2 bis 3 Proc.
Zinn und nur einige Tausendtheile Schwefel und Eisen enthielt. Dieses Resultat
hat uns nicht überrascht; der Arsenik kann nur durch eine große Reihe auf
einander folgender Operationen (Röstungen und Reductionen) fast vollständig
entfernt werden. Daher ist denn auch der beschriebene Proceß für Erze welche
viel Arsenik oder Antimon enthalten, wie z.B. Fahlerz, nicht geeignet.
Mit Kiesen, die nicht arsenikhaltig sind, haben wir immer ein sehr reines
Schwarzkupfer erhalten, welches nur 3 bis 5 Tausendtheile Schwefel enthielt.
Mehrere von unsern Zainen zeigten eine deutliche seidenartige Textur.
Bei einem Versuch haben wir einen Zuschlag von Schweißofen-Schlacken der
Eisenhütte zu Grenelle gemacht, welche sehr viele Schüppchen von metallischem
Eisen enthielten, wodurch unser Kupfer einen Eisengehalt von 3 Procent bekam.
Die Eisenschüppchen wurden sogleich von dem Kupfer aufgenommen und vereinigten
sich auf der Sohle, konnten sich daher nicht in der Schlacke auflösen. Aus
diesem Grunde haben wir es auch unterlassen Versuche mit Feilspänen von
Schmiede- oder Gußeisen als Ersatzmittel der Eisenstäbe anzustellen, weil
sich ein Theil dieser Späne offenbar mit dem Kupfer verbunden hätte.
Die Röstung hat einen gewissen Einfluß auf das Ergebniß an Kupfer, sowie auf den
Abgang oder Verbrauch des Eisens. Waren die Erze gut abgeröstet, so haben wir
nie einen Stein über dem Kupfer gehabt, was hingegen bei unvollkommen gerösteten Erzen
stets der Fall war, wenn auch in geringem Grade. Das Schwarzkupfer enthielt
durchaus kein Eisen, und weniger als 0,008 Schwefel. Der Eisenabgang war etwas
größer als mit denselben Erzen bei guter Röstung und die zuletzt gefallene
Schlacke etwas reicher.
Die zweckmäßigste Temperatur ist nach unserer Erfahrung die zur Schmelzung des
Kupfers und der Schlacke durchaus nothwendige. Eine höhere Temperatur erhöht die
schnelle Einwirkung des Eisens auf das Kupfersilicat, allein die Kohle reducirt
auch einen Theil des mit der Kieselerde verbundenen Eisenoxyds leichter. Indem
wir auf gleiche Weise dasselbe Erz in einer mäßigen Temperatur und in einer sehr
starken Rothglühhitze behandelten, erhielten wir im ersten Falle sehr reines
Kupfer und im zweiten Fall Kupfer mit 3 Procent Eisengehalt.
Der Kohlenverbrauch unseres Ofens zur Erzielung der erforderlichen Temperatur
liefert durchaus keinen Anhaltspunkt hinsichtlich des Steinkohlenquantums, das
ein großer Flammofen bei ununterbrochenem Betriebe erfordern würde.
Die Erze bei denen unser Verfahren am besten anwendbar ist, sind oxydirte oder
kiesige, deren Gangarten Eisenkies oder Brauneisenstein sind; sie geben mittelst
unserer Schmelzmethode ein sehr gutes Kupfer und kommen leicht in Fluß. Macht
man diese Erze im Krummofen zu Gute, so producirt man ein sehr eisenhaltiges
Kupfer. Unsere Methode läßt sich auch sehr gut auf alle Kupfererze anwenden, die
nicht viel Arsenik oder Antimon enthalten, ferner auf reiche Schlacken
u.s.w.
Man ersieht aus Obigem, daß der beschriebene Kupferschmelzproceß gegen die
gewöhnlich angewendeten mehrere wesentliche Vortheile gewährt; er zeichnet sich
durch Schnelligkeit und Wohlfeilheit aus, da man beim Schmelze eine so arme
Schlacke erhält, daß sie über die Halde gestürzt werden kann, und ein
hinlänglich reines Kupfer, um es nach dem Garmachen sogleich in den Handel
bringen zu können. Ueberdieß hat dieser Schmelzproceß gar keine Schwierigkeiten
und jeder Arbeiter ist sehr bald im Stande ihn zu erlernen und auszuführen. Eine
vollständige Röstung ist ein so bekannter Hüttenproceß, daß er keiner weitern
Beschreibung bedarf; er ist besonders leicht, wenn das Erz in Schliech
verwandelt ist. Von Seiten des Arbeiters erfordert er Gewandtheit und
Aufmerksamkeit, und muß mit einer starken Hitze geschlossen werden, um die in
einer niedrigen Temperatur gebildeten schwefelsauren Salze zu zersetzen. – Die
Verwandlung eines Erzes, welches in Stufen gewonnen wird, in Schliech, so wie
die Röstung im Flammofen selbst, können durch eine vorhergehende Röstung in
Haufen, welche nur unbedeutende Kosten verursacht, wesentlich erleichtert
werden. – Wir haben schon oben bemerkt, daß die Hauptnachtheile einer
unvollständigen Röstung bei der Schmelzung ein weit größerer Eisenabgang, sowie
eine weit reichhaltigere Schlacke sind.
Ein guter Röstofen müßte ungefähr 1500 Kilogr. oder 30 Centner Schliech aufnehmen
können. Die Operation würde ungefähr 15 bis 18 Stunden dauern. Zur Schmelzung
müßte man Oefen anwenden, die den großen Waliser Schmelzöfen ähnlich sind, und
eine Ladung von 1200 Kilogr. oder 24 Centner aufnehmen können. Zu drei
Schmelzöfen würden vier Röstöfen erforderlich seyn, vorausgesetzt daß man in
jedem Schmelzofen drei Operationen machen will. – Das Garmachen des bei
dem Schmelzen gewonnenen Schwarzkupfers würde sehr zweckmäßig in einem Flammofen
vorgenommen werden können, welcher 4000 Kilogr. aufnehmen kann, und es würde
eine solche Operation nicht über zwölf Stunden Zeit erfordern.“
Bezüglich des Kostenpunkts dieses Kupferschmelzprocesses verweisen wir auf
den Eingangs erwähnten Bericht von Pelouze.
Tafeln